Comment des systèmes chimiques peuvent-ils mimer la sélection naturelle ?
Si de nombreuses réactions chimiques sont réversibles, la reproduction des êtres vivants se fait, elle, à sens unique de manière irréversible. Ce principe essentiel, mais habituellement ignoré, rend possible la sélection naturelle. Afin de mieux comprendre comment le lien entre irréversibilité et évolution est apparu en biologie, des chercheurs du CNRS et d’Aix-Marseille Université ont décrit, de manière conceptuelle, une réaction chimique qui se produirait de façon irréversible et déboucherait sur un mécanisme de réplication moléculaire, imitant la sélection naturelle connue dans le monde biologique. Ces travaux, publiés dans Nature Reviews Chemistry, précisent certaines conditions environnementales nécessaires à la transition inerte-vivant.
La présence de matière organique ne suffit pas à l’apparition de la vie. Le passage de la chimie à la biochimie demande un contexte bien particulier, que la recherche tente de mieux définir. Un des points importants est l’irréversibilité. En effet, la reproduction des êtres vivants est à sens unique : deux cellules venant de se séparer ne peuvent en aucun cas refusionner en rendant leurs précurseurs chimiques. La sélection naturelle a besoin de ce principe, fixant les gènes avant de les sélectionner. Ce comportement diffère de celui des particules de la physique statistique microscopique, toujours décrites par des équations réversibles. Des chercheurs du laboratoire Physique des interactions ioniques et moléculaires (PIIM, CNRS/Aix-Marseille Université) ont publié les premiers contours théoriques d’un processus chimique de réplication irréversible. Ils montrent ainsi que la sélection naturelle, moteur du darwinisme, prendrait bien naissance dans le monde moléculaire de la matière « inerte ».
Leur modèle repose sur une réaction autocatalytique dans laquelle la stœchiométrie mène globalement à deux entités d’un catalyseur C par réaction d’un réactif R via l’intermédiaire I. Pour être irréversible, la formation de I doit se dérouler avec un apport d’énergie tel que la réaction retour soit impossible avant l’apparition des deux catalyseurs. Sinon, ce serait comme si l’information génétique était perdue avant que la reproduction ait lieu. Les chercheurs ont ensuite estimé l’énergie nécessaire pour faire fonctionner un tel système à la température de l’eau liquide, et montré que la lumière visible, par exemple celle du Soleil dans un environnement naturel, convient. La combinaison de la photochimie et d’un milieu aqueux serait donc essentielle pour l’origine moléculaire d’une auto-organisation moléculaire, selon un processus permettant ensuite l’émergence du vivant, à partir d’un système chimique maintenu loin de l’équilibre. Les chercheurs vont à présent tester expérimentalement leurs hypothèses, en quête de réactions qui y répondent dans un environnement donné, compatible avec celui qui aurait pu exister sur la Terre au moment de l’émergence du vivant.
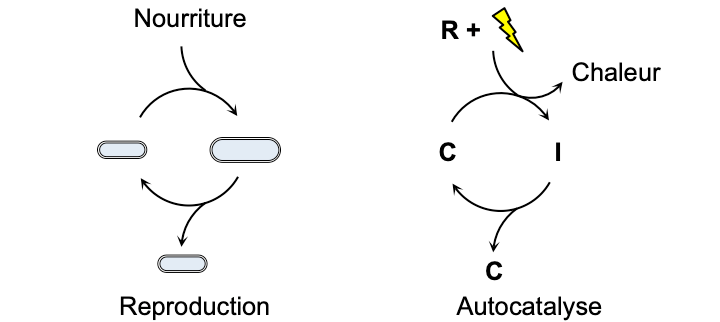
Cycle cellulaire dans lequel la cellule croît puis se divise et au sein duquel l’irréversibilité s’exprime par des transformations unidirectionnelles. Ce cycle cellulaire est comparé à un système chimique autocatalytique en prenant en compte la nécessité d’une irréversibilité associée à la dissipation d’énergie sous forme de chaleur et menant à la production d’entropie.
Référence
On the conditions for mimicking natural selection in chemical systems,
G. Danger, L. Le Sergeant d’Hendecourt and R. Pascal
Nature Reviews Chemistry, volume 4, pages 102–109. (2020)
doi.org/10.1038/s41570-019-0155-6