Détection rapide d'un biomarqueur du cancer par une puce microfluidique
Des chercheurs du LAAS-CNRS, en collaboration avec le Centre de recherche en cancérologie de Toulouse, ont montré comment la technologie de puce microfluidique μLAS permettait de concentrer et mesurer en moins d'une minute des micro-ARN, biomarqueurs de cancers.
Les micro-ARN (miR) sont des courts fragments d'ARN qui jouent un rôle dans l'expression des gènes. Leur concentration est fortement altérée chez les patients atteints d'un cancer, et c'est pourquoi les miR sont une cible de choix pour le diagnostic et le suivi des malades, à condition de disposer d'une méthode de détection et de mesure suffisamment sensible et rapide pour être utilisée cliniquement. Des chercheurs du LAAS-CNRS, en collaboration avec le Centre de recherche en cancérologie de Toulouse, ont effectué une percée importante dans cette direction, en réalisant la détection du miR-21 en moins d'une minute grâce à une puce microfluidique. Ces résultats sont publiés dans la revue Biosensors and Bioelectronics.
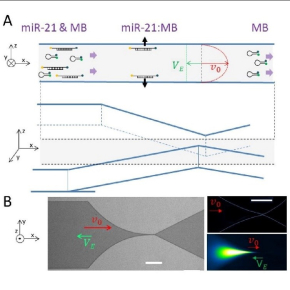
La technologie de puce microfluidique μLAS permet de concentrer et séparer des acides nucléiques de tailles ciblées. La solution contenant les micro-ARN, couplés avec des sondes moléculaires fluorescentes, est envoyée dans un canal microfluidique en forme d'entonnoir, tandis qu'une force électrophorétique1 est créée à contre-courant. En ajustant la pression et la tension électrique, la molécule à concentrer s'accumule en un point du microcanal. Des mesures de fluorescence sont alors réalisées en ce point en plaçant la puce sur un microscope optique.
Afin de tester une utilisation clinique de cette technique, le dispositif a été employé pour mesurer la concentration de miR-21 à partir de prélèvement par biopsie sur des patients atteints du cancer du pancréas. Les mesures effectuées ont montré que les résultats étaient cohérents avec ceux obtenus par la méthode d'analyse d'ARN qui aujourd'hui fait référence (RT-PCR). De plus, la technologie μLAS atteint une sensibilité de 2 pM (picomole/L) en 30 secondes, ce qui représente un bon compromis entre rapidité de mesure et sensibilité, comparé aux technologies aujourd'hui utilisées.
Les chercheurs s'attachent maintenant à augmenter encore la sensibilité de la technologie. Celle-ci pourrait s'accroître d'un facteur 1000, en optimisant la géométrie de la puce microfluidique, afin d'améliorer la précision des tests de suivi de micro-ARN.
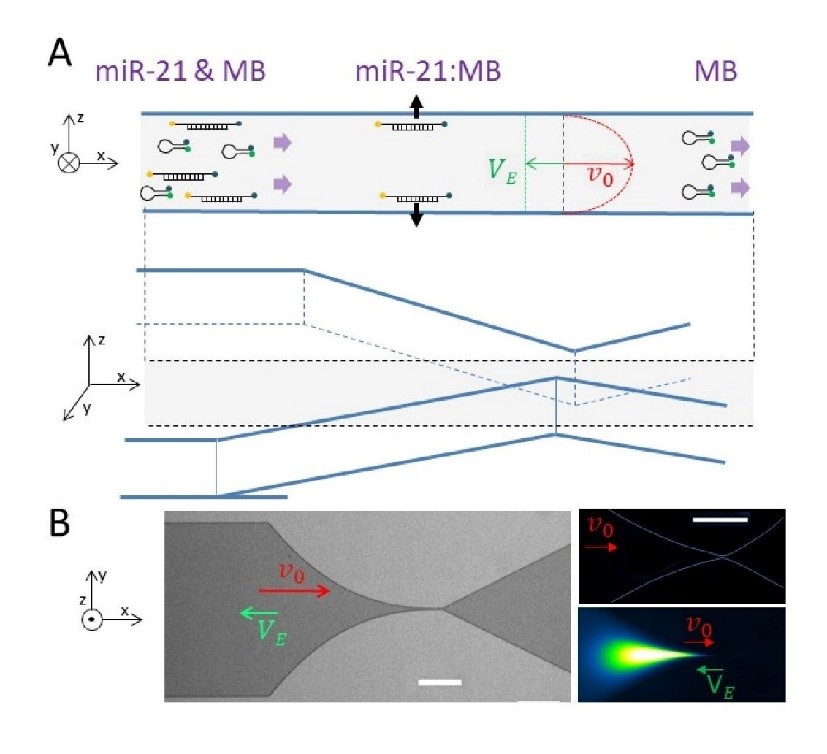
(B) Le panneau de gauche montre une photographie optique de l'entonnoir (les barres d'échelle correspondent à 200 microns).
Les deux images de droite correspondent à des clichés de microscopie de fluorescence avec la condition initiale (champ hydrodynamique seul, panneau du haut) et champ électrique simultané après 30 secondes de concentration (panneau du bas)
© Aurélien Bancaud, LAAS-CNRS
Références
Micro-RNA 21 detection with a limit of 2 pM in 1 min using a size-accordable concentration module operated by electrohydrodynamic actuation
I. Tijunelyte, R. Malbec, B. Chami, J. Cacheux, C. Dez, T. Leichlé, P. Cordelier, A. Bancaud.
Biosensors and Bioelectronics Volume 178, 15 April 2021
DOI: 10.1016/j.bios.2021.112992
DNA separation and enrichment using electro-hydrodynamic bidirectional flows in viscoelastic liquids
H. Ranchon, R. Malbec, V. Picot, A. Boutonnet, P. Terrapanich, P. Joseph, T. Leïchlé, A. Bancaud
Lab on a Chip (2016) 16: 1243-1253.
DOI : 10.1039/c5lc01465d
A tunable filter for high molecular weight DNA selection and linked-read sequencing
N. Milon, J.L.F. Rojas, A. Castinel, L. Bigot, G. Bouwmans, K. Baudelle, A. Boutonnet, A. Gibert, O. Bouchez, C. Donnadieu, F. Ginot, A. Bancaud
Lab on a Chip (2020) 20: 175-184.
DOI : 10.1039/C9LC00965E
- 1L'électrophorèse consiste à faire migrer des espèces chimiques chargées, comme les acides nucléiques, sous l'action d'un champ électrique.